传统肺癌微生物组研究高度依赖16S rDNA测序等非培养技术,难以获得活菌株开展功能验证。本研究整合培养组学 + 16S rDNA 高通量测序 + 体外功能实验,首次从临床肺癌组织中分离可培养菌株,并证实其促肿瘤增殖、促炎的关键作用,为肺癌微生物机制研究与靶向干预提供核心实验依据。

发表期刊:BMC Microbiology(IF=4.2)
发表时间:2025年8月
DOI:10.1186/s12866-025-04237-4
核心技术:培养组学 | 16S rDNA 测序 |体外功能验证
1.用培养组学 + 16S rDNA测序,鉴定肺癌组织驻留微生物;
2.体外验证分离得到菌株功能,明确其与肺癌发展的关联机制。
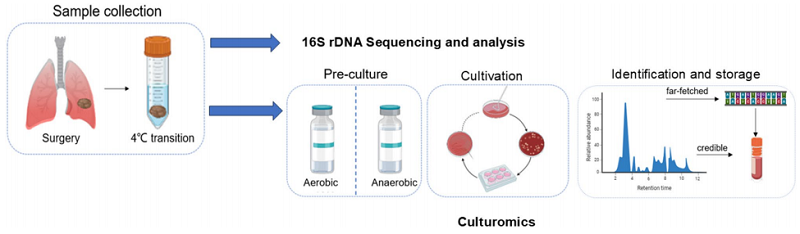
实验设计与培养组学方法、流程总结
1.样本收集与处理:选取未手术/未放化疗的NSCLC患者,术中取肿瘤组织1-4cm3。一份用于细菌培养组学分析,新鲜样本冰上1h内送实验室处理;另一份-80℃保存,用于16S rDNA测序。同时设置环境和培养对照,排除污染干扰。
1)16S rDNA测序分析:扩增16S rRNA的V3-V4区,通过测序平台进行双端测序;经聚类OTU(97%相似性)、Silva数据库物种注释,分析肺癌组织微生物的群落组成。
2)培养组学分析:将肿瘤组织匀浆后预培养于5%血培养瓶,分别在1、3、6天取样,梯度稀释后接种于5%绵羊血哥伦比亚琼脂,同时进行有氧培养(37℃,24h)和厌氧培养(37℃,72h);对菌落进行鉴定,对鉴定结果不佳的菌株进行16S rRNA全长测序。
1)菌株筛选:选取4种葡萄球菌菌株(S.warneri-01、S.hominis-22、S.capitis-22、S.nepalensis-09),以健康人粪便分离的鼠李糖乳杆菌为阴性对照。
2)肿瘤细胞增殖检测:采用RTCA(实时细胞分析)技术监测A549肺癌细胞。
3)促炎细胞因子检测:ELISA检测上清液中TNF-α、IL-1β、IL-6等促炎细胞因子。
18份样本中5份培养阳性,细菌平均检出率27.8%,共分离鉴定出12种细菌,葡萄球菌属占比最高(59%);厌氧条件下分离的菌株数量多于有氧条件,初始培养阶段为菌株分离的最佳窗口期。
2)16S rDNA测序的微生物组成
门水平的变形菌门、厚壁菌门、放线菌门占主导;样本间个体差异极大,肿瘤微环境菌群高度异质性。

16SrRNA测序鉴定的肺癌组织细菌组成分析
A.18例肺癌样本在门水平的分类组成;B.18例肺癌样本在属水平的分类组成
培养组学分离的12种细菌分属厚壁菌门(67%)、放线菌门(25%)、变形菌门(8%),与测序的菌门组成趋势一致;但仅芽孢杆菌属能同时通过两种方法检出,其余菌属存在明显检测差异,提示肿瘤微生物的培养难度较高。
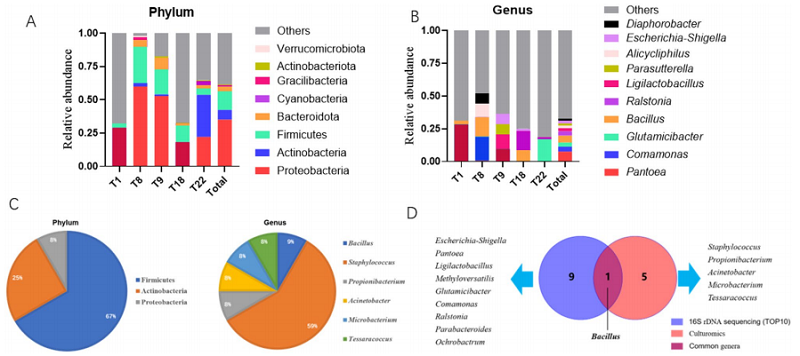
16S rDNA 测序与培养组学方法的比较
A 5例培养阳性肺癌样本中丰度前10菌门的百分比直方图;
B 5例培养阳性肺癌样本中丰度前10菌属的百分比直方图;
C 5例肺癌样本中分离的12种细菌按门与属划分的百分比构成;
D 18例样本测序丰度前10菌属与5例样本可分离菌属的对比
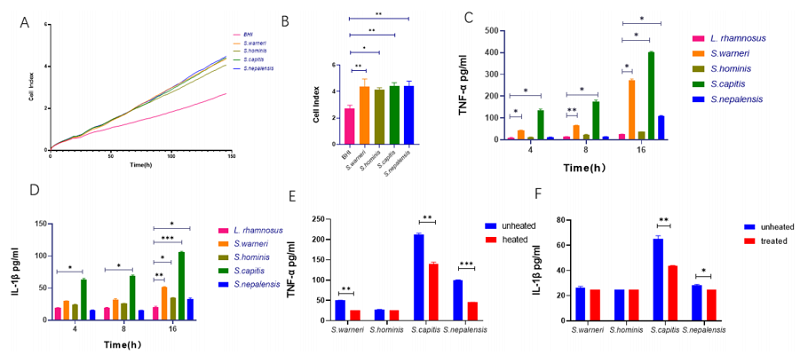
体外增殖与促炎作用检测
A实时细胞分析检测不同葡萄球菌株对肺癌细胞系增殖的促进作用;
B刺激148小时后细胞指数统计分析;C四株菌与THP-1共培养上清中TNF-α含量;
D四株菌与THP-1共培养上清中IL-1β含量;E加热组与未加热组四株菌上清中TNF-α含量;
F加热组与未加热组四株菌上清中IL-1β含量。
本研究联用测序+培养组学分析肺癌组织菌群:测序可揭示微生物组成,培养组学既能部分验证测序结果,更能获得可用于后续研究的活菌;研究首次通过培养法从肺癌组织分离菌株并完成体外功能验证。
微基生物可提供肿瘤微生物样本处理、有氧/厌氧分离培养、16S rDNA测序与菌株精准鉴定、细菌培养上清代谢物分析等服务,并围绕肿瘤微生物研究特点,提供实验设计、样本采集、方法选择及结果解析的全流程技术咨询,助力提升菌株分离效率与功能验证准确性。

 微基生物 您自己的微生态研究团队|专注微生态研究与应用
微基生物 您自己的微生态研究团队|专注微生态研究与应用



