肿瘤微生物研究 全流程解决方案:高通量测序+分离培养+原位验证

一、研究概况
2024年发表于Nature Communications(IF=17.694) 的重磅研究,首次证实鼻咽癌患者存在「口腔→鼻咽」微生物异常易位,明确具核梭杆菌(Fusobacterium nucleatum)、中间普雷沃菌(Prevotella intermedia)等关键菌株,揭示微生物与EBV协同促进鼻咽癌发生发展机制,为鼻咽癌肿瘤微生态研究、早期筛查与靶向干预提供核心依据。
文章标题:Microbes translocation from oral cavity to nasopharyngeal carcinoma in patients(口腔微生物向鼻咽癌患者肿瘤组织的移位)
二、严谨实验设计(肿瘤微生物多队列+多技术闭环验证)
1.研究队列设计
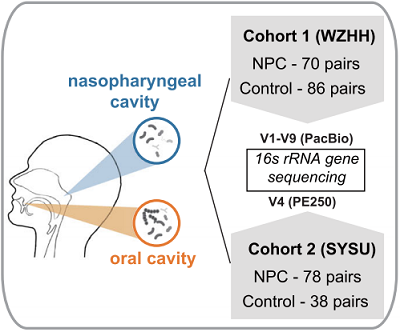
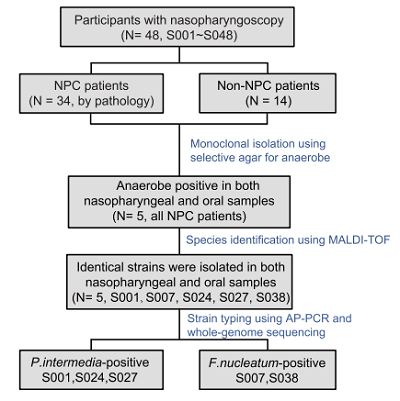
NPC病例对照微生物组研究设计 培养组学研究流程设计
发现队列(Cohort 1):70例NPC患者+86例健康对照,配对鼻咽拭子+口腔唾液样本,PacBio全长16S测序,进行物种水平分析。
验证队列(Cohort 2):78例NPC患者+38例健康对照,Illumina 16S V4测序,进行属水平验证。
培养组学队列:48例受试者(34例NPC患者+14例对照),配对鼻咽拭子和唾液样本,进行微生物分离培养与菌株鉴定。
转录组验证队列:101例受试者组织(89例NPC患者+12例对照),宏转录组测序。
2.核心技术与检测目的(全流程解析)
|
实验技术 |
方法 |
研究目的 |
|
16S rRNA测序 |
PacBio全长、Illumina V4 |
解析口腔/鼻咽菌群组成、差异与来源追踪 |
|
微生物培养组 |
厌氧培养、选择性培养基 |
分离纯化菌株,验证口腔→鼻咽易位 |
|
AP–PCR/全基因组 |
菌株分型、ANI分析 |
确认口腔与鼻咽为相同菌株 |
|
宏转录组测序 |
菌群定位+宿主表达分析 |
验证肿瘤内定植、重塑微环境 |
|
FISH荧光原位杂交 |
通用细菌探针+种特异性探针 |
原位示踪具核梭杆菌/中间普雷沃菌 |
|
qPCR定量 |
EBV BamHI–W区域定量 |
检测鼻咽EBV载量,关联微生物丰度 |
三、肿瘤微生物关键研究结果
结果1:鼻咽癌患者口腔–鼻咽微生物生态位消失
健康人群中,鼻咽部优势菌为棒状杆菌属、葡萄球菌属、痤疮皮肤杆菌属;口腔优势菌为链球菌属、奈瑟菌属、普雷沃菌属,微生物群组成差异显著;NPC患者中,两个部位的微生物群组成相似度显著升高(P<0.001),提示微生物生态位特异性丧失。
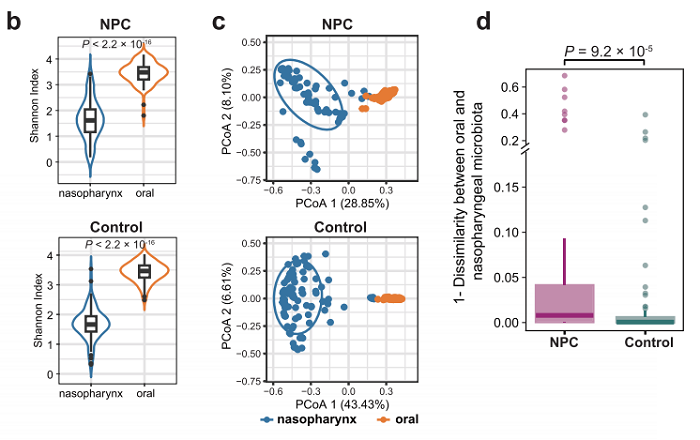
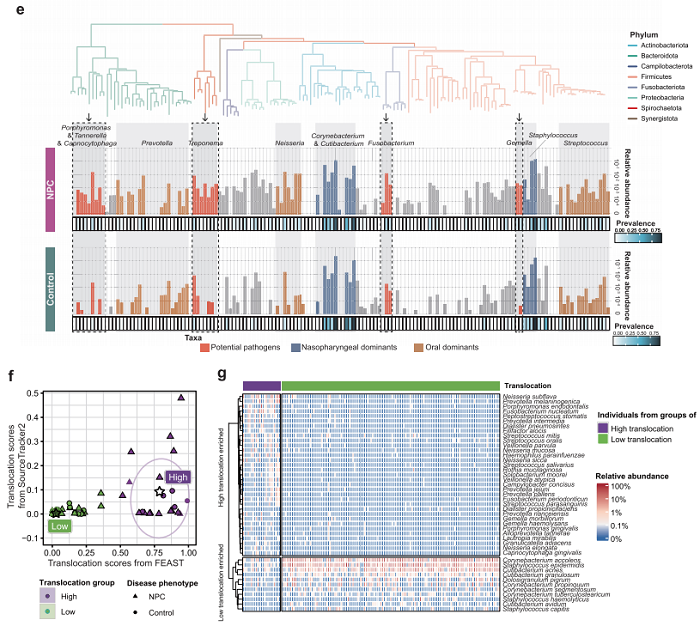
图1b:鼻咽菌群α多样性显著低于口腔;
图1c/d:PCoA分析显示NPC患者两部位菌群更趋近,组成相似性远高于对照组;
图1e:NPC 鼻咽富集口腔致病菌,共生菌显著减少;
图1f/g:高易位组 NPC 风险是低易位组4.51倍(OR=4.51,P=0.012)
结果2:口腔→鼻咽微生物易位显著升高鼻咽癌风险
来源追踪分析显示,NPC患者的口腔微生物向鼻咽部移位评分显著高于对照组;高移位组的NPC发病风险是低移位组的4.51倍(95%CI:1.47-16.04,P=0.012);筛选出33种高移位组富集物种(以口腔优势菌为主)和11种depletion物种(以鼻咽部共生菌为主)。
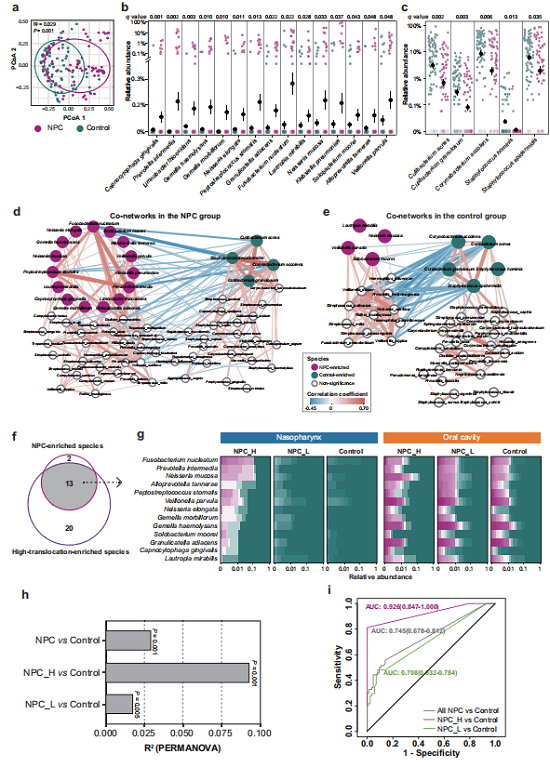
图2a:NPC与对照鼻咽菌群结构显著分离;
图2b/c:NPC富集口腔致病菌,耗竭棒状杆菌、表皮葡萄球菌等共生菌;
图2d/e:NPC组口腔致病菌形成强正相关共生网络,对照组网络松散;
图2f–i:13种核心菌精准定义高风险亚型,诊断效能优异。
结果3:培养组学菌株水平实锤口腔→鼻咽微生物易位
培养组学验证:在2例NPC患者中分离到鼻咽部与口腔同源的具核梭杆菌菌株,3例患者中分离到同源的中间普雷沃菌菌株,全基因组ANI分析证实跨部位菌株高度同源(99.999%),彻底证实易位真实存在。
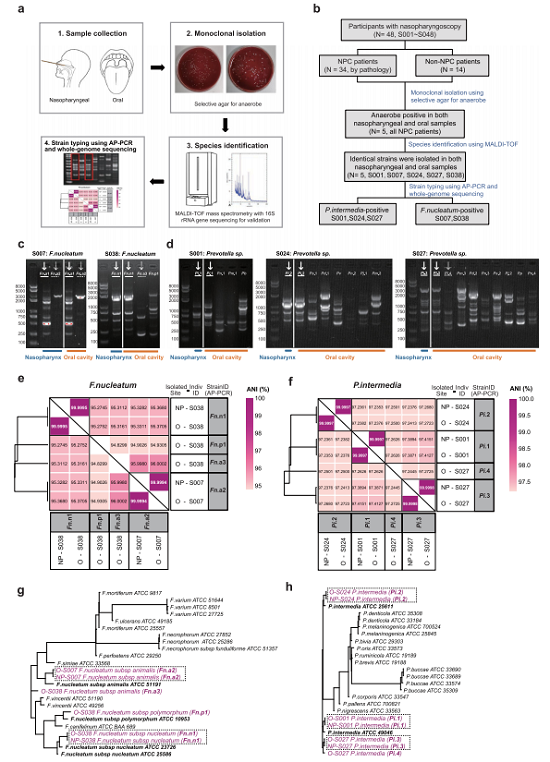
图3a–d:厌氧培养从NPC患者鼻咽与口腔分离到完全相同菌株。
图3e–h:ANI 值与进化树双重证实跨部位菌株同源,易位真实存在。
结果4:易位微生物侵入肿瘤内部,重塑促瘤免疫微环境
FISH和宏转录组证实,9/13种核心易位菌定植于肿瘤组织中,具核梭杆菌在NPC患者中的检出率(29.2%)显著高于对照组(8.3%),中间普雷沃菌仅在肿瘤组织中检出(10.1%);
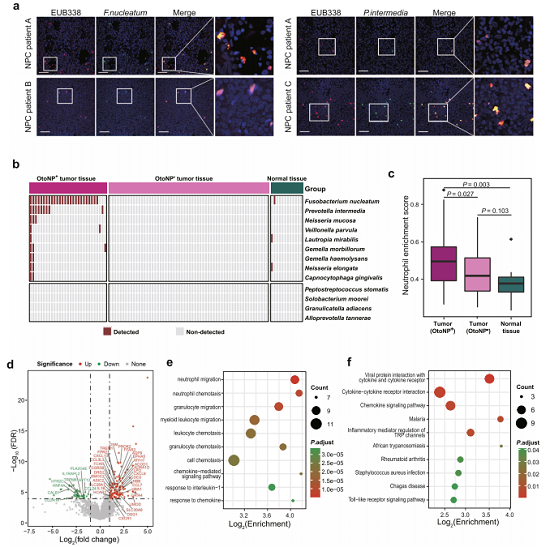
图4a:FISH证实具核梭杆菌、中间普雷沃菌定植于NPC肿瘤组织;
图4b:宏转录组验证 9 种核心易位菌存在于 NPC 肿瘤内;
图4c:易位菌阳性肿瘤组织中中性粒细胞显著富集;
图4d:易位菌调控宿主基因表达,上调促炎与中性粒细胞相关基因;
图4e:差异基因富集于中性粒细胞趋化、迁移等促炎通路;
图4f:差异基因富集病毒-细胞因子互作通路,提示微生物与EBV协同作用。
结果5:易位微生物与EBV载量呈显著正相关
EBV载量与移位微生物数量呈剂量依赖关系(EBV高载量组移位物种数显著高于低载量组,P=6.6×10-5);6种NPC_OtoNP易位菌与EBV载量呈正相关,其中具核梭杆菌相关性最强(R=0.36,P=4.2×10-6);鼻咽部共生菌(如Accolens棒状杆菌)与EBV载量呈负相关,且对口腔微生物移位具有保护作用。
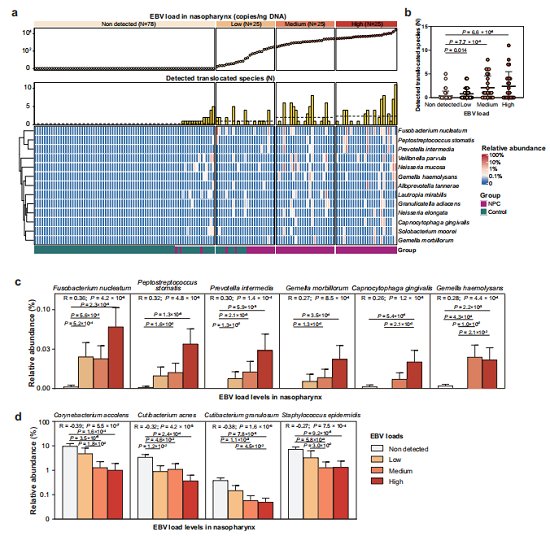
图5a–b:EBV载量越高,检出易位菌种数越多。
图5c:具核梭杆菌、中间普雷沃菌等6种NPC_OtoNP菌种与EBV载量强正相关。
图5d:鼻咽共生菌与EBV载量负相关,发挥定植抵抗作用。
微基生物专注肿瘤微生物组研究,拥有成熟的厌氧培养平台、高通量测序平台、FISH原位验证平台、多组学分析平台,具备完整技术体系,助力肿瘤微生物机制研究与高分文章发表!

 微基生物 您自己的微生态研究团队|专注微生态研究与应用
微基生物 您自己的微生态研究团队|专注微生态研究与应用



