肿瘤内微生物群是调控肿瘤发生发展、转移及治疗响应的关键因子。在肺癌、肝癌、胆管癌多种实体瘤中,特异性微生物群落通过重塑免疫微环境、调控代谢通路等方式影响肿瘤生物学行为。但因其低丰度与环境复杂性使分离培养与精准检测极具挑战。
微基生物依托高通量培养组学平台与专属培养基体系,搭建分离培养+FISH原位验证全流程服务,可对肺癌、肝癌、胆管癌、宫颈癌等多种实体瘤组织开展功能菌株的分离、鉴定与定位验证,形成完整研究闭环。
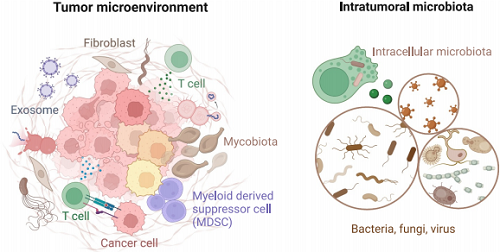
肿瘤微环境与肿瘤内微生物群示意图
一、常见肿瘤微生物样本类型
肿瘤微生物研究的样本类型覆盖组织、体液及专属特色样本,不同样本可从不同维度解析肿瘤微生物的分布、功能及与机体的关联,为多方位研究提供样本支撑。
肿瘤组织样本:原发性肿瘤组织、转移性肿瘤组织及癌旁正常组织,是直接解析肿瘤微环境中微生物群落组成与功能的核心样本。常见类型有肺癌组织、肝癌组织、宫颈癌组织、乳腺癌组织、胰腺癌组织、胃癌组织等。
体液样本:血液、腹水、胸腔积液、胆汁、十二指肠液等,可用于探究肿瘤微生物的全身性分布及转移特征,为液体活检相关研究提供支撑。
其他样本:口腔癌患者的口腔黏膜样本、结直肠癌患者的粪便样本等,可用于分析肿瘤微生物的来源及与机体微生态系统的关联。
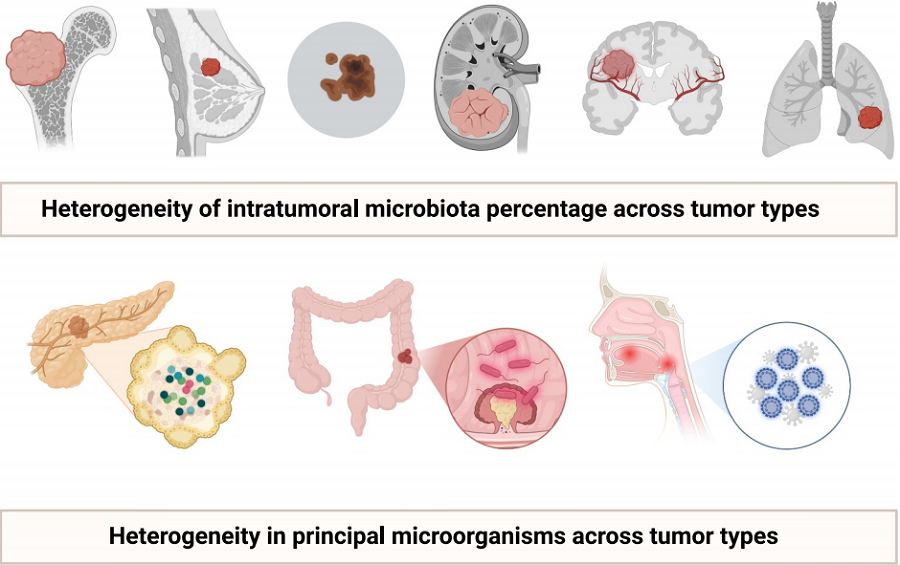
不同肿瘤类型的肿瘤微生物示意图
二、肿瘤微生物科研核心方向及研究现状
当前肿瘤微生物研究已从菌群组成分析,迈向单菌株功能验证与空间定位的新阶段。微基生物在提供测序服务之外,更专注于肿瘤样本的微生物分离培养,并搭配高灵敏、高特异性 FISH 技术,为科研提供从菌株获取到原位验证的完整解决方案。
1)肿瘤微生物核心研究方向

核心技术支撑:分离培养 + FISH原位验证双技术体系
2)部分肿瘤样本分离菌株及主要功能研究
|
肿瘤类型 |
菌株名称 |
主要功能 |
参考文献 |
|
肝内胆管癌(ICC) |
Paraburkholderia fungorum、Staphylococcus capitis |
P.fungorum在癌旁组织富集,与CA199负相关,通过调控氨基酸代谢抑制胆管癌细胞增殖与迁移;S.capitis可抑制胆管癌细胞划痕愈合与迁移。 |
[2] |
|
结直肠癌(CRC) |
Bacteroides fragilis |
与Faecalibacterium prausnitzii在结直肠癌微环境中相互拮抗,通过代谢产物或信号通路调控肠道炎症与肿瘤细胞增殖。 |
[3] |
|
肝癌 |
Klebsiella pneumoniae |
通过表面蛋白PBP1B激活TLR4通路,促进细胞增殖与致癌信号,加速肝癌进展;破坏肠道屏障,易位至肝脏定植。 |
[4] |
|
肺腺癌 |
Staphylococcus nepalensis、Staphylococcus capitis |
在肺腺癌转移灶富集,与复发、不良预后相关;通过分泌乳酸激活 MCT1-假缺氧-NDRG1轴,增强肿瘤细胞迁移与侵袭能力,敲除乳酸合成基因可抑制转移。 |
[5] |
|
宫颈癌 |
Lactobacillus iners |
在宫颈肿瘤中富集,与放化疗抵抗、复发风险升高及生存期缩短相关;分泌L-乳酸重编程肿瘤代谢,增强癌细胞对放化疗的抵抗能力。 |
[6] |
注意:所有肿瘤相关菌株的分离均需严格控制无菌操作、设置阴性对照,结合FISH检测验证菌株原位定位,避免污染干扰。微基生物可根据不同肿瘤类型及菌株特性,提供全流程分离培养与功能验证服务,助力科研人员高效开展研究。
三、文献案例 肿瘤驻留葡萄球菌通过乳酸介导的信号轴促进转移定植
文献:Yu H, et al. Lactate production by tumor-resident Staphylococcus promotes metastatic colonization in lung adenocarcinoma. Cell Host & Microbe, 2025.
该研究首次揭示,肿瘤驻留葡萄球菌(S.nepalensis和S.capitis)通过分泌乳酸激活MCT1-假性缺氧-NDRG1信号轴促进肺腺癌(LUAD)转移定植的分子机制,其中微生物组学分析为研究发现核心肺腺癌转移关联菌属奠定了关键实验基础。
(一)微生物组学分析技术
1.16S rRNA基因测序:对LUAD患者原发灶、转移淋巴结、非转移淋巴结样本进行16S rRNA基因高通量测序,完成菌群组成的初步筛选;
2.微生物培养组学:采用多培养条件(好氧/厌氧+5%羊血/5%瘤胃液)对LUAD原发灶新鲜样本进行富集培养,分离获得患者来源的纯细菌菌株;
3.荧光原位杂交(FISH):采用葡萄球菌特异性Cy5标记探针,对福尔马林固定石蜡包埋(FFPE)样本进行杂交染色,判定葡萄球菌阳性阈值(Cy5阳性面积>0.9%);
4.实时荧光定量PCR(qPCR):采用葡萄球菌特异性Taqman探针,以S.nepalensis为阳性对照建立标准曲线,定量临床样本中葡萄球菌的DNA含量,实现葡萄球菌丰度的精准定量。
(二)微生物组学检测结果
16S rRNA基因测序:明确葡萄球菌为LUAD转移灶特异性富集菌属
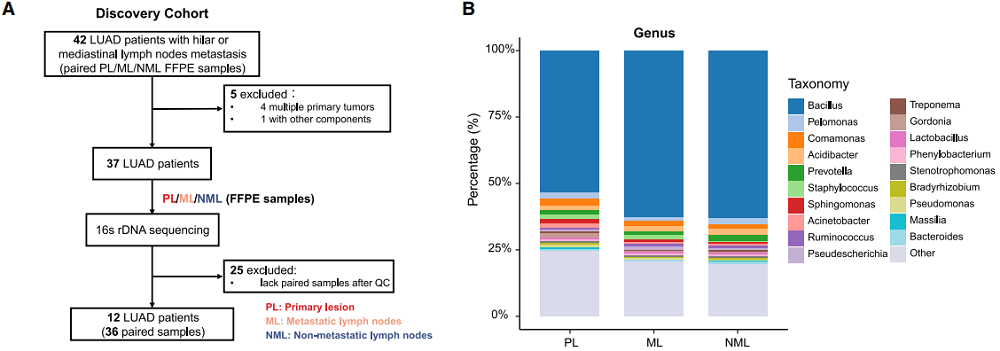
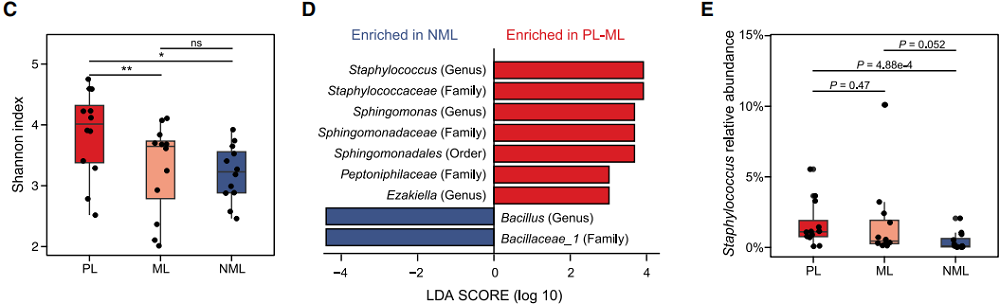
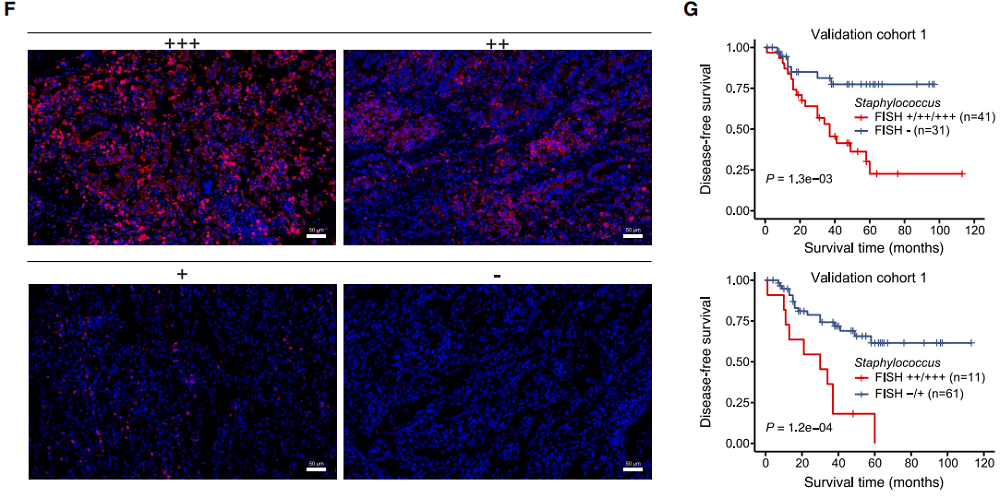
图A:发现队列样本排除标准流程图;图B:菌属水平菌群相对丰度堆叠图;
图C:Shannon指数α多样性箱线图;图D:LEfSe分析差异富集菌属图;
图E:葡萄球菌在不同样本中的相对丰度箱线图;图F:葡萄球菌特异性FISH染色图片;
图G:不同葡萄球菌丰度LUAD患者的Kaplan-Meier无病生存期(DFS)曲线。
检测结论:16S rRNA基因测序结合FISH/qPCR验证,明确了葡萄球菌在LUAD原发灶和转移淋巴结中特异性富集,且其丰度与患者复发风险升高、无病生存期缩短显著相关,是LUAD转移的关键关联菌属。
微生物培养组学:从LUAD肿瘤组织中分离获得葡萄球菌菌株
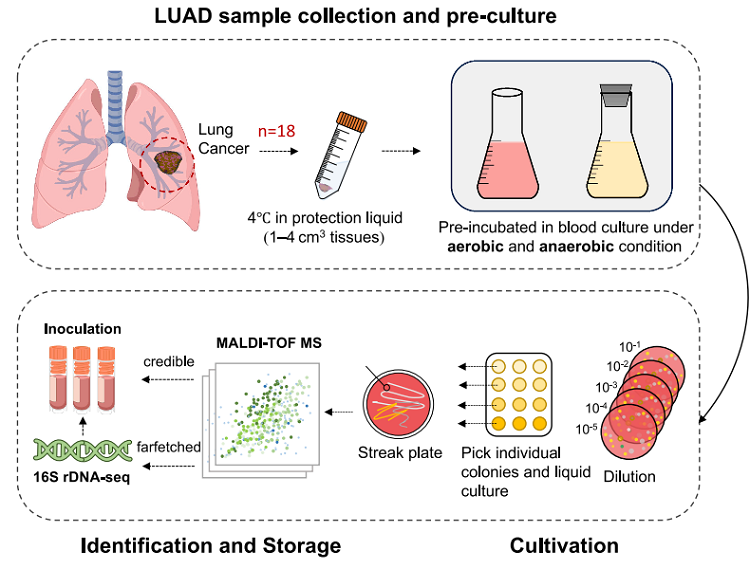
微生物培养组学技术流程图
检测结论:对18例LUAD原发灶新鲜样本进行多条件富集培养与鉴定,成功分离获得12株纯细菌菌株,其中6株为葡萄球菌属;结合功能实验筛选出4株具有促转移潜能的菌株,其中S.nepalensis和S.capitis的促转移效应最显著。
靶向验证:葡萄球菌在LUAD远处转移灶中存在且与复发相关
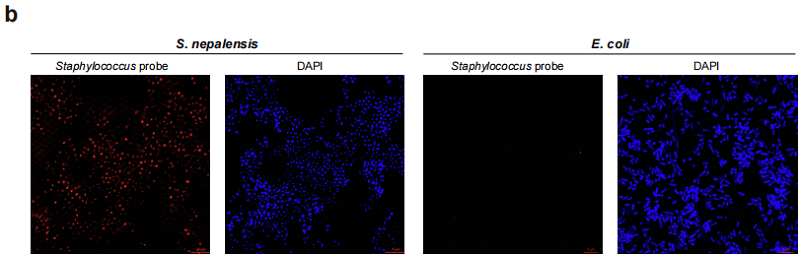
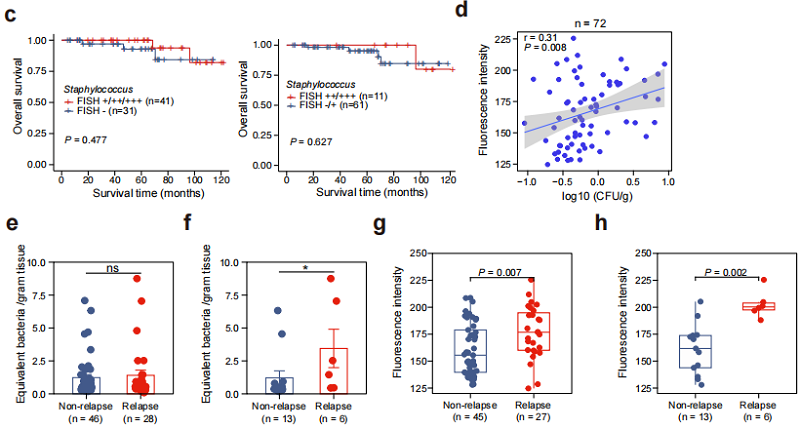
(b) 荧光原位杂交(FISH)探针标记的尼泊尔葡萄球菌和大肠杆菌荧光图像
(c) 肺腺癌患者总生存期(OS)的 Kaplan-Meier生存曲线(验证队列 1)
(d) 荧光定量 PCR(qPCR)检测的葡萄球菌载量与FISH荧光强度的相关性散点图
(e, f) 验证队列1中不同复发状态肺腺癌患者的葡萄球菌载量qPCR定量柱状图
(g, h) 验证队列1中不同复发状态肺腺癌患者的葡萄球菌FISH荧光强度柱状图
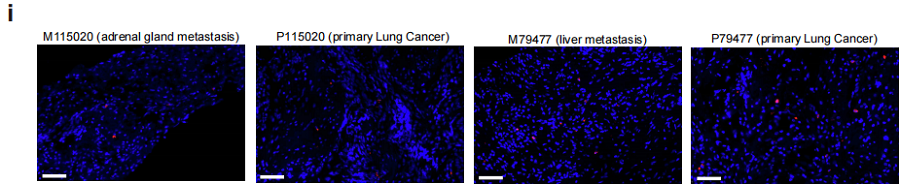
(i) 2 例肺腺癌患者原发灶与配对转移灶中葡萄球菌的代表性FISH图像
检测结论:qPCR与FISH检测均证实,术后12个月内复发的LUAD患者肿瘤组织中葡萄球菌丰度显著高于无复发生存超5年的患者(均 P<0.05);在LUAD患者肾上腺、肝脏等远处转移灶中检测到葡萄球菌信号,证实葡萄球菌可随LUAD细胞发生远处转移。
以上研究通过16S rRNA基因测序、培养组学、FISH/qPCR靶向验证的多维度微生物组学分析技术,实现了“筛选差异菌属-分离活菌菌株-验证临床关联”的完整研究链条。
四、微基生物全方位优势

参考文献
1.Gao Z, et al. Heterogeneity of intratumoral microbiota in tumor microenvironment and tumor development. Med Research, 2025.
2.Chai X, et al. Intratumor microbiome features reveal antitumor potentials of intrahepatic cholangiocarcinoma. Gut Microbes, 2023.
3.Kong C, et al. Antagonistic interactions of Faecalibacterium prausnitzii and Bacteroides fragilis in CRC. Gastroenterology, 2026.
4.Yu J, et al. Gut-liver translocation of Klebsiella pneumoniae promotes HCC. Nature Microbiology, 2025.
5.Yu H, et al. Lactate production by tumor-resident Staphylococcus promotes metastatic colonization in lung adenocarcinoma. Cell Host & Microbe, 2025.
6.Colbert L E, et al. Tumor-resident Lactobacillus iners confer chemoradiation resistance via lactate-induced metabolic rewiring. Cancer Cell, 2023.
7.Zepeda-Rivera M A, et al. Fusobacterium sphaericum sp. nov., isolated from human colon tumor, adheres to colonic epithelial cells and induces IL-8 secretion. Gut Microbes, 2025.

 微基生物 您自己的微生态研究团队|专注微生态研究与应用
微基生物 您自己的微生态研究团队|专注微生态研究与应用




